Commissione Europea approva ruxolitinib, crema per il trattamento della vitiligine
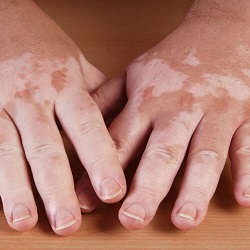
Il prodotto da 15 mg/g di Incyte valido per il trattamento della vitiligine non segmentale con coinvolgimento del viso in adulti e adolescenti a partire dai 12 anni di età
La Commissione Europea ha concesso l’autorizzazione all’immissione in commercio per ruxolitinib crema 15 mg/g di Incyte nel trattamento della vitiligine non segmentale con coinvolgimento del viso in adulti e adolescenti a partire dai 12 anni di età.
Ruxolitinib crema è il primo e unico trattamento approvato nell’Unione Europea a offrire supporto per la ripigmentazione in pazienti idonei con vitiligine non segmentale, una malattia autoimmune cronica caratterizzata da depigmentazione della pelle e ridotta qualità della vita.
pubblicità
La decisione della CE fa seguito al parere positivo ricevuto all’inizio del 2023 dal Comitato per i medicinali per uso umano (CHMP) dell’Agenzia Europea per i Medicinali (EMA) ed è applicabile a tutti i 27 Stati membri dell’Unione Europea, all’Islanda, alla Norvegia e al Liechtenstein.
“L’approvazione di ruxolitinib crema da parte della Commissione Europea rappresenta un progresso significativo per le persone che vivono con vitiligine non segmentale con coinvolgimento facciale che, fino ad ora, non avevano alcun trattamento medico approvato per indurre la ripigmentazione”, osserva Hervé Hoppenot, CEO di Incyte. “Questa approvazione non sarebbe stata possibile senza il supporto dei pazienti affetti da vitiligine e della comunità medica e senza gli sforzi dei nostri team di ricerca e sviluppo. Ora lavoreremo nei singoli Paesi europei per portare questa tanto attesa terapia ai pazienti idonei che cercano di trattare la propria vitiligine”.
La decisione della Commissione Europea si basa sui dati di due studi clinici registrativi di fase 3 – TRuE-V1 e TRuE-V2 – che hanno valutato l’efficacia e la sicurezza di ruxolitinib crema rispetto al veicolo (crema non medicata) in più di 600 persone con vitiligine non segmentale, di età pari o superiore a 12 anni.
I risultati del programma TRuE-V hanno dimostrato che il trattamento con ruxolitinib crema ha determinato miglioramenti significativi nella ripigmentazione facciale e di tutto il corpo rispetto al veicolo, come dimostrato dal numero di pazienti che hanno raggiunto gli endpoint dell’indice di punteggio dell’area della vitiligine facciale e corporea totale (Facial and Total body Vitiligo Area Scoring Index – F-VASI and T-VASI) alla settimana 24 rispetto al veicolo e, in un’estensione in aperto, alla settimana 52.
I risultati alla settimana 24, coerenti in entrambi gli studi, hanno mostrato che il 29,8% e il 30,9% dei pazienti trattati con ruxolitinib crema ha ottenuto un miglioramento di almeno il 75% rispetto al basale nell’indice di punteggio dell’area della vitiligine facciale (F-VASI75), l’endpoint primario, rispetto al 7,4% e 11,4% dei pazienti trattati con il veicolo rispettivamente in TRuE-V1 e TRuE-V2. Alla settimana 52, dei pazienti trattati con ruxolitinib crema ha raggiunto la risposta F-VASI75 circa un paziente su due.
Inoltre, alla settimana 24, oltre il 15% dei pazienti trattati con ruxolitinib crema ha ottenuto un miglioramento ≥90% rispetto al basale nel punteggio F-VASI (F-VASI90) rispetto a circa il 2% dei pazienti trattati con veicolo. Alla settimana 52, dei pazienti trattati con ruxolitinib crema ha raggiunto una risposta F-VASI90 circa un paziente su 3. Non ci sono stati eventi avversi gravi correlati al trattamento con ruxolitinib crema e la reazione avversa più comune è stata acne nella sede di applicazione. I dati degli studi registrativi di fase III a sostegno della decisione della Commissione Europea sono stati anche pubblicati dal The New England Journal of Medicine.
“L’approvazione di ruxolitinib crema è una buona notizia per i dermatologi e i pazienti idonei in Europa che spesso affrontano difficoltà nella gestione della vitiligine”, afferma Markus Böhm, Dipartimento di Dermatologia, Università di Münster, Germania. “TRuE-V è il primo programma di studi clinici su larga scala per la vitiligine e i suoi risultati dimostrano chiaramente i miglioramenti clinicamente significativi nella ripigmentazione facciale e corporea totale osservati con ruxolitinib crema e il suo potenziale per ottimizzare ulteriormente la cura e gli esiti nei pazienti.”
La vitiligine è una malattia autoimmune cronica caratterizzata da depigmentazione della pelle che si traduce in una perdita a chiazze del colore della pelle in seguito alla progressiva distruzione delle cellule produttrici di pigmento, note come melanociti. Si ritiene che l’iperattività della via di segnale JAK guidi l’infiammazione coinvolta nella patogenesi e nella progressione della vitiligine.
Nell’Unione Europea, nei Paesi del SEE e nel Regno Unito si stima che la prevalenza della vitiligine diagnosticata sia di circa 1,5 milioni di pazienti di cui circa 8 su 10 soffrono di vitiligine non segmentale, e un sottogruppo di questi presenta un coinvolgimento del viso e richiede un trattamento. La vitiligine può verificarsi a qualsiasi età, anche se molti pazienti con vitiligine manifestano i primi sintomi prima dei 30 anni.
“La vitiligine è una malattia autoimmune cronica che ha un impatto su molti aspetti della vita di una persona”, conclude Jean-Marie Meurant, Vicepresidente del Comitato Internazionale delle Organizzazioni dei Pazienti affetti da Vitiligine (VIPOC). “L’arrivo di nuove opzioni terapeutiche è importante per la nostra comunità, perché offre alle persone affette da vitiligine ciò che speravano da tempo: la possibilità di scegliere di trattare la propria patologia.”
I Correlati
L’esposizione alle radiazioni solari o alle fonti artificiali è il “driver” principale dell’insorgenza dei tumori della pelle
Pubblicate sull’European Journal of Cancer le raccomandazioni stilate da esperti provenienti da 5 continenti e da società scientifiche internazionali
Incontro Aifa-Egualia, Nisticò: Al lavoro per assicurare che tutti i farmaci essenziali siano disponibili per i pazienti italiani
“La lotta al fenomeno delle carenze passa anche attraverso il riconoscimento delle necessità di rendere economicamente sostenibili molti farmaci essenziali. Siamo al lavoro su questo aspetto”
Obesità: semaglutide 2,4 mg riduce il rischio di eventi cardiovascolari avversi maggiori
La riduzione del rischio di MACE è stata raggiunta indipendentemente dal livello di peso basale, dall'indice di massa corporea (BMI), dalla circonferenza vita e dal rapporto vita/altezza
Uda, progetto sistemi intelligenti per somministrazione farmaci
Allo studio nuovi sistemi di nanoparticelle per contrastare lo sviluppo di biofilm microbici responsabili di gravi infezioni
Ti potrebbero interessare
Obesità: semaglutide 2,4 mg riduce il rischio di eventi cardiovascolari avversi maggiori
La riduzione del rischio di MACE è stata raggiunta indipendentemente dal livello di peso basale, dall'indice di massa corporea (BMI), dalla circonferenza vita e dal rapporto vita/altezza
Uda, progetto sistemi intelligenti per somministrazione farmaci
Allo studio nuovi sistemi di nanoparticelle per contrastare lo sviluppo di biofilm microbici responsabili di gravi infezioni
Da ospedali a farmacie via libera a 200 farmaci: cure facilitate ai diabetici
Prima tranche per la riforma che riguarda milioni di malati
I dati di efficacia a sei anni di Ofatumumab di Novartis mostrano benefici sostanziali nelle persone con sclerosi multipla recidivante
Il trattamento con ofatumumab fino a sei anni continua a essere ben tollerato con risultati di sicurezza coerenti, a sostegno del profilo beneficio-rischio favorevole di ofatumumab nella SMR
Ultime News
L’esposizione alle radiazioni solari o alle fonti artificiali è il “driver” principale dell’insorgenza dei tumori della pelle
Pubblicate sull’European Journal of Cancer le raccomandazioni stilate da esperti provenienti da 5 continenti e da società scientifiche internazionali
Lesioni tumorali ai polmoni, messa a punto una nuova tecnica per agire rapidamente
Radiologi e clinici del Policlinico Gemelli hanno ideato un metodo per 'taggare' con una piccola spirale metallica (microcoil) queste lesioni
Esofagite eosinofila, boom di casi. Studio Usa: negli ultimi 30 anni più 800 per cento
Di natura infiammatoria cronica e progressiva, è provocata da un “corto circuito” del sistema immunitario. Interessa l’esofago causandone il restringimento. La sua principale conseguenza è che diventa difficile, a volte impossibile, la deglutizione
In Italia circa 600 mila le persone celiache di cui circa il 60% non ancora diagnosticate
Fino al 19 maggio AIC promuove la Settimana Nazionale della Celiachia per informare, sensibilizzare e offrire sostegno ai malati e ai loro familiari








Commenti